Ácidos carboxílicos são compostos orgânicos que têm em sua estrutura o grupo carboxila. Nesse sentido, apresentam um carbono que acaba se ligando (ligação dupla) com oxigênio e com o grupo OH (ligação simples).
O ácido carboxílico designa uma função orgânica oxigenada, ou seja, possui um átomo de oxigênio em sua estrutura. Por serem ácidos, por característica própria, apresentam capacidade de corrosão e o típico sabor azedo.
Todavia, a carboxila é representada por COOH e representa a união estabelecida entre o grupo carbonila (C=O) e hidroxila (OH). O ácido mais antigo de que se tem notícia é o ácido acético (CH3COOH), que dá origem ao vinagre.
Este composto é uma solução aquosa, com 4% a 7% de ácido acético, formado pela fermentação aeróbica de várias bebidas alcoólicas, a partir da ação de bactérias. Todavia, bebidas alcoólicas com menos de 7% de álcool azedam em contato com o ar (fermentação alcoólica).
Nomenclatura dos ácidos carboxílicos
A nomenclatura dos ácidos carboxílicos pode ser feita pelo prefixo, seguido do tipo de ligação, mais o sufixo OICO. Nesse sentido, para nomear um ácido carboxílico, é necessário seguir esses passos:
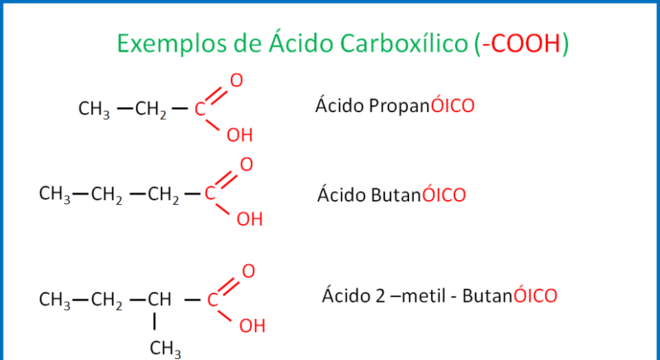
Primeiro deve vir o prefixo, observando sempre o número de carbonos existentes na cadeia. Posteriormente, é necessário verificar quantas ligações existem na cadeia, e ao final adicionar o sufixo OICO.
Nesse sentido, cada tipo de ligação tem uma terminação diferente na hora de nomear os ácidos carboxílicos. Assim, cadeias com ligações simples levam ‘AN’ no nome; ligações duplas acrescentam ‘EN’ em seus nomes e, por fim, ligações triplas com a terminação ‘IN’.
Todavia, as insaturações e ramificações de cada cadeia devem sempre ser numeradas, iniciando-se sempre pela extremidade mais próxima do seu grupo funcional, neste caso o grupo carboxila.
Alguns exemplos de nomenclatura:
Ácido Metanoico – met (um carbono na cadeia) + an (ligação simples) + oico Etanoico – et (dois carbonos na cadeia) + an (ligação simples) + oico Propanoico – prop (três carbonos) + an (ligação simples) + oicoNesse sentido, de acordo com o número de carbonos, os ácidos recebem a seguinte nomenclatura: met, para um carbono; et, dois carbonos; prop, casos de 4 carbonos; pent; hex; hept; oct e mon, respectivamente.
Características dos ácidos
Os ácidos carboxílicos possuem características bem específicas. De forma geral, são solúveis em solventes orgânicos, sendo os únicos solúveis em água, aqueles que possuem até quatro átomos de carbono.
Todavia, são mais densos que a água, exceto os ácidos com um ou dois átomos de carbono. Em temperatura ambiente, os ácidos com até nove carbonos estão em estado líquido. No geral, os ácidos em estado sólido são esbranquiçados e se assemelham à uma cera; já em estado líquido são incolores.
Assim, como apresentam carboxila, são capazes de se ligar com o hidrogênio. E em geral, os ácidos carboxílicos são inodoros, com exceção dos que possuem até três carbonos, que apresentam um cheiro irritante e os de seis carbonos, conhecidos pelo cheiro insuportável e repugnante.
Aplicabilidade dos ácidos carboxílicos
Os ácidos carboxílicos são dotados de várias funções, sendo aplicados e usados na produção de ésteres orgânicos e na produção de sais de ácidos carboxílicos.
Todavia, são usados para a fabricação de perfumes, de vinagres, de seda artificial e desinfetantes. Na indústria têxtil, eles são usados para o tingimento de tecidos.

Então, o que achou da matéria? Se gostou, leia também: Pontes de hidrogênio, o que são? Definição, características e aplicação.
Fontes: Brasil Escola, Info Escola, Toda Matéria, Manual da Química
Imagens: Quora, Química, Docsity, Ph-metros 10, Cozinha Técnica
Essa matéria Ácidos carboxílicos – Nomenclatura, características e aplicabilidade foi criada pelo site Conhecimento Científico.


![Primos fazem SEXO e causa polemica [VÍDEO COMPLETO E SEM TARJAS]](http://3.bp.blogspot.com/-vXjTwuHUrsE/Un_88dXnSrI/AAAAAAAADyM/wxGcIRXYVz4/w72-h72-p-k-no-nu/Sem+t%C3%ADtulo.jpg)



0 Comentários